Arbeitsgruppe Professor Jaster
1. Zelluläre Seneszenz im Kontext von Pankreasfibrose und Pankreaskarzinom
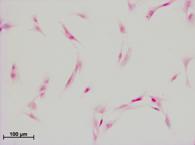
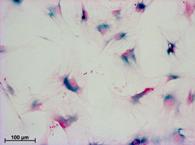
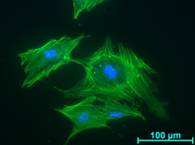
Die chronische Pankreatitis und das Pankreaskarzinom werden von einer Organfibrose begleitet, die auf die Aktivierung pankreatischer Sternzellen (PSZ) zurückgeht und bisher nicht behandelbar ist. Ziel unserer Arbeiten ist es, die molekularen Grundlagen des Prozesses zu charakterisieren und experimentelle Therapiestrategien zur gezielten Modulation des bindegewebigen Organumbaus zu entwickeln. Die Arbeitsgruppe hat hierzu in vitro und in vivo Modelle entwickelt, die sich sowohl für Studien zur Pathophysiologie als auch zur Erprobung potenzieller Behandlungsmöglichkeiten eignen. Aktuell stehen in den Arbeiten Mechanismen der PSZ-Seneszenz im Vordergrund. Dahinter steht die Hypothese, dass Störungen der Zellalterung sowie von Wechselwirkungen zwischen gealterten PSZ und Zellen des Immunsystems maßgeblich an der Entstehung der Fibrose beteiligt sind. Die molekularen Grundlagen der Sternzelleseneszenz und die pathophysiologischen Konsequenzen des Seneszenzprozesses wurden von uns anhand experimenteller Modell im Detail analysiert (Fitzner et al. 2012). Als ein Schlüsselmediator der Sternzellseneszenz konnte der Zellzyklusinhibitor CDKN1A identifiziert werden (Fitzner et al. 2013, Müller et al. 2016). In unseren aktuellen Studien untersuchen wir zusätzlich auch an experimentellen Modellen des Pankreaskarzinoma Seneszenzprozesse und -mechanismen. Dabei geht es um die Frage, ob die Kombination aus einer gezielten Seneszenzinduktion und der nachfolgenden Lyse seneszenter Tumorzellen therapeutisches Potenzial besitzt (Revskij et al. 2023 und 2024).
2. Pathophysiologische Grundlagen der Autoimmunpankreatitis
Die autoimmune Pankreatitis (AIP) ist eine eher seltene Sonderform der chronischen Entzündung der Bauchspeicheldrüse. Ihre Erforschung ist dennoch wichtig, da die Erkrankung schwer zu diagnostizieren ist und eine andere Behandlung erfordert als die häufigeren Verlaufsformen. Die Arbeitsgruppe untersucht anhand eines Mausmodells die Grundlagen der AIP und erprobt im Tierversuch neue Therapieansätze, die auf dem Einsatz moderner Immunsuppressiva beruhen. In Zusammenarbeit mit Kooperationspartnern konnte dabei u.a. gezeigt werden, dass Ciclosporin A und Rapamycin im Tierxperiment eine ähnlich gute therapeutische Wirksamkeit erzielen wie Steroide (Schwaiger et al. 2014). Ein weiteres Ziel besteht in der Identifizierung von Genen, die den Ausbruch der Erkrankung begünstigen. Hier gelang der Arbeitsgruppe in Zusammenarbeit mit Kooperationspartnern ein Durchbruch, indem erstmals quantitative trait loci (QTL) der experimentellen AIP kartiert und anschließend in Beziehung zu den immunologischen Grundlagen der Erkrankung gesetzt werden konnten (Asghari et al. 2011; Bischof et al. 2015; Borufka et al. 2016; Ehlers et al. 2018). In Weiterführung dieser Arbeiten gelang es, zwei neue Risikogene der AIP zu identifizieren (Jaster et al. 2020). Derzeit erproben wir in experimentellen Studien Substanzen mit Anwendungspotenzial in der Humanmedizin, die diese Risikogene adressieren (Agrifoglio et al. 2024).
3. Anwendungen von Systembiologie/Bioinformatik in der Erforschung von Pankreaserkrankungen
In den letzten Jahren konnten wichtige Signaltransduktionswege, die für die Entstehung und Entwicklung des Pankreaskarzinoms sowie der begleitenden Fibrose von Bedeutung sind, identifiziert werden. Bis heute sind die Zusammenhänge auf molekularer Ebene jedoch unzureichend verstanden. In einem interdisziplinären Projektansatz entwickeln wir in Kooperation mit Partnern aus der Systembiologie und Bioinformatik auf Basis experimenteller Daten Modelle, um vorrangig folgende Fragen zu beantworten: Wie sind die einzelnen rezeptorvermittelten Signalwege miteinander verknüpft? Welche Schritte in den Signalkaskaden sind geschwindigkeitslimitierend? Lassen sich sensitive Parameter identifizieren, die als Ansatz für neue Therapien von Interesse sein können? Die bisherigen Studien der Arbeitsgruppe haben u.a. zu neuen Einblicken in die Wirkmechanismen von Interferon-gamma geführt, eines Zytokins, das sowohl auf die Tumor- als auch auf die Bindegewebszellen wachstumshemmende Effekte entfaltet (Rateitschak et al. 2010, Lange et al. 2011). Zusätzlich dazu untersuchten wir Mechanismen der epithelial-mesenchymalen Transition; eines zentralen Mechanismus in der Tumorprogession (Rateitschak et al. 2016). Der interdisziplinäre Ansatz wurde von uns auch auf experimentelle Studien zur akuten Pankreatitis und hierbei speziell zur Rolle freier Radikale im Entzündungsprozess ausgedehnt. Dabei gelang uns u.a. der Nachweis, dass ein Knockout des uncoupling protein 2 Gens in Mäusen nicht nur mit einer höheren ROS-Belastung, sondern auch mit einem etwas schwereren Verlauf der experimentellen Cerulein-Pankreatitis einhergeht (Müller et al. 2014). In unseren aktuellen Studien zu Mechanismen der Seneszenz und Senolyse im Kontext des Pankreaskarzinoms und der Pankreasfibrose kooperieren wir ebenfalls eng mit Partnern aus der Bioinformatik und Systembiologie (Revskij et al. 2023 und 2024).
4. Die Arbeitsgruppe ist außerdem mit experimentellen Studien am Verbundprojekt EnErGie und als Laborpartner an den klinischen Studien der Abteilung beteiligt.
Ausgewählte Publikationen der Arbeitsgruppe:
1. Agrifoglio O, Kasprick A, Gross N, Wahlig M, Kauffold E, Woitas A, Vorobyev A, Ehlers L, Ludwig RJ, Bieber K, Jaster R. Dexamethasone's Clinical Efficacy in Experimental Autoimmune Pancreatitis Correlates with a Unique Transcriptomic Signature, Whilst Kinase Inhibitors Are Not Effective. Biomedicines. 2024 Oct 29;12(11):2480. https://pubmed.ncbi.nlm.nih.gov/39595046/
2. Revskij D, Woitas A, Kölle B, Umstätter C, Zechner D, Khan FM, Fuellen G, Jaster R. Effects of triggers of senescence and senolysis in murine pancreatic cancer cells. Hepatobiliary Pancreat Dis Int. 2024 Dec;23(6):628-637.https://pubmed.ncbi.nlm.nih.gov/38879414/
3. Revskij D, Runst J, Umstätter C, Ehlers L, Rohde S, Zechner D, Bastian M, Müller-Hilke B, Fuellen G, Henze L, Murua Escobar H, Junghanss C, Kowald A, Walter U, Köhling R, Wolkenhauer O, Jaster R. Uncoupling protein 2 deficiency of non-cancerous tissues inhibits the progression of pancreatic cancer in mice. Hepatobiliary Pancreat Dis Int. 2023 Apr;22(2):190-199. https://pubmed.ncbi.nlm.nih.gov/36549966/
4. Jaster R, Gupta Y, Rohde S, Ehlers L, Nizze H, Vorobyev A, Ludwig RJ, Ibrahim SM. Impact of diet and genes on murine autoimmune pancreatitis. J Cell Mol Med. 2020 Aug;24(15):8862-8870. https://pubmed.ncbi.nlm.nih.gov/32643288/
5. Elleisy N, Rohde S, Huth A, Gittel N, Glass Ä, Möller S, Lamprecht G, Schäffler H, Jaster R. Genetic association analysis of CLEC5A and CLEC7A gene single-nucleotide polymorphisms and Crohn’s disease. World J Gastroenterol. 2020:26(18):2194-2202. https://www.wjgnet.com/1007-9327/full/v26/i18/2194.htm
6. Ehlers L, Rohde S, Ibrahim S, Jaster R. Adoptive transfer of CD3(+) T cells and CD4(+) CD44(high) memory T cells induces autoimmune pancreatitis in MRL/MpJ mice. J Cell Mol Med. 2018 Apr;22(4):2404-2412.https://www.ncbi.nlm.nih.gov/pubmed/29383850
7. Wallbaum P, Rohde S, Ehlers L, Lange F, Hohn A, Bergner C, Schwarzenböck SM, Krause BJ, Jaster R. Antifibrogenic effects of vitamin D derivatives on mouse pancreatic stellate cells. World J Gastroenterol. 2018 Jan 14;24(2):170-178. https://www.ncbi.nlm.nih.gov/pubmed/29375203
8. Rohde S, Lindner T, Polei S, Stenzel J, Borufka L, Achilles S, Hartmann E, Lange F, Maletzki C, Linnebacher M, Glass Ä, Schwarzenböck SM, Kurth J, Hohn A, Vollmar B, Krause BJ, Jaster R. Application of in vivo imaging techniques to monitor therapeutic efficiency of PLX4720 in an experimental model of microsatellite instable colorectal cancer. Oncotarget. 2017 Jul 15;8(41):69756-69767. https://www.ncbi.nlm.nih.gov/pubmed/29050239
9. Borufka L, Volmer E, Müller S, Engelmann R, Nizze H, Ibrahim S, Jaster R. In vitro studies implicate an imbalanced activation of dendritic cells in the pathogenesis of murine autoimmune pancreatitis. Oncotarget. 2016 Jul 12;7(28):42963-42977. https://www.ncbi.nlm.nih.gov/pubmed/27356751
10. Rateitschak K, Kaderali L, Wolkenhauer O, Jaster R. Autocrine TGF-β/ZEB/microRNA-200 signal transduction drives epithelial-mesenchymal transition: Kinetic models predict minimal drug dose to inhibit metastasis. Cell Signal. 2016 Aug;28(8):861-70. https://www.ncbi.nlm.nih.gov/pubmed/27000495
11. Bischof J, Müller S, Borufka L, Asghari F, Möller S, Holzhüter SA, Nizze H, Ibrahim SM, Jaster R. Quantitative Trait Locus Analysis Implicates CD4⁺/CD44high Memory T Cells in the Pathogenesis of Murine Autoimmune Pancreatitis. PLoS One. 2015 Sep 1;10(9):e0136298. https://www.ncbi.nlm.nih.gov/pubmed/26325540
12.Fitzner B, Lange A, Müller S, Jaster R. Cdkn1a is a key mediator of rat pancreatic stellate cell senescence. Pancreatology. 2013 May-Jun;13(3):254-62. https://www.ncbi.nlm.nih.gov/pubmed/23719597
13. Schwaiger T, van den Brandt C, Fitzner B, Zaatreh S, Kraatz F, Dummer A, Nizze H, Evert M, Bröker BM, Brunner-Weinzierl MC, Wartmann T, Salem T, Lerch MM, Jaster R, Mayerle J. Autoimmune pancreatitis in MRL/Mp mice is a T cell-mediated disease responsive to cyclosporine A and rapamycin treatment. Gut. 2014 Mar;63(3):494-505. https://www.ncbi.nlm.nih.gov/pubmed/23564336
14. Fitzner B, Müller S, Walther M, Fischer M, Engelmann R, Müller-Hilke B, Pützer BM, Kreutzer M, Nizze H, Jaster R. Senescence determines the fate of activated rat pancreatic stellate cells. J Cell Mol Med. 2012 Nov;16(11):2620-30. https://www.ncbi.nlm.nih.gov/pubmed/22452900
15. Asghari F, Fitzner B, Holzhüter SA, Nizze H, de Castro Marques A, Müller S,Möller S, Ibrahim SM, Jaster R. Identification of quantitative trait loci for murine autoimmune pancreatitis. J Med Genet. 2011 Aug;48(8):557-62. https://www.ncbi.nlm.nih.gov/pubmed/21709168
Mitarbeiter:
Prof. Dr. med. Robert Jaster, Laborleiter
Frau Dr. rer. hum. Luise Ehlers
Frau Ottavia Agrifoglio, M.Sc.
Frau Katja Bergmann, BTA
sowie Studenten der Medizinischen Biotechnologie und der Humanmedizin im Rahmen der Bearbeitung von Bachelorarbeiten und Promotionsthemen.

